Tỉ khối hơi và công thức tính tỉ khối hơi chất khí là phần kiến thức rất quan trọng khi bắt đầu học và tìm hiểu về chất khí. Bài viết dưới đây sẽ củng cố cho bạn những kiến thức về tỉ khối hơi là gì? và công thức tính tỉ khối hơi chất khí, từ đó đưa ra các bài tập vận dụng liên quan đến tỉ khối hơi. Mời các bạn cùng theo dõi!
Tỉ khối hơi là gì?
Tỉ khối hơi là một khái niệm chỉ được sử dụng cho những chất khí. Trong đó có thể hiểu đây là công thức tính khốii lượng mol của khí này để so sánh với khối lượng mol của khí kia. Từ đó ta có thể xác định được khí nào nặng hơn hay nhẹ hơn bao nhiêu so với khí còn lại.

Tỉ khối hơi so với không khí
Cũng tương tự như định nghĩa trên thì tỉ khối hơi so với không khí là công thức tính khối lượng mol của không khí với khối lượng mol của khí còn lại.
Tỉ khối hơi so với heli
Tỉ khối hơi của một khí so với heli là khối lượng mol của khí đó so với khối lượng mol của heli
Tỉ khối hơi so với Oxi
Tỉ khối hơi của một khí so với oxi là khối lượng mol của khí đó so với khối lượng mol của Oxi.
Xem thêm: NaHCO3 là muối gì? NaHCO3 có kết tủa không? ứng dụng của NaHCO3
Công thức tính tỉ khối hơi chất khí
Để tính được tỉ khối hơi chất khí ta có công thức như sau:
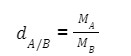
Theo đó:
d : là tỉ khối của chất khí A so với tỉ khối của chất khí B
M : là khối lượng mol của chất khí A
M: là khối lượng mol của chất khí B

Áp dụng công thức trên chúng ta cũng có thể tính nhanh được công thức tỉ khối hơi của một khí so với không khí, heli hay oxi. Chẳng hạn như ta có công thức tỉ khối hơi của khí A với không khí, heli, oxi như sau:
Công thức tính tỉ khối hơi so với không khí: d = M/ 29
Công thức tính tỉ khối so với heli: d = M / 4
Công thức tính tỉ khối so với oxi: d = M / 32
Sau khi đã biết được công thức tính tỉ khối chất khí, từ đó chúng ta có thể xác định sự nhẹ hơn hay nặng hơn bao nhiêu lần giữa chúng.
Chẳng hạn như 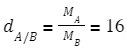 ; ta có thể kết luận rằng khí A nặng hơn khí B 16 lần.
; ta có thể kết luận rằng khí A nặng hơn khí B 16 lần.
Xem thêm: FeCl3 màu gì? Tính chất hóa học và ứng dụng của FeCl3
Bài tập vận dụng
Để hiểu hơn về định nghĩa và công thức tính tỉ khối hơi chất khí mình sẽ cùng nhau giải bài tập vận dụng dưới đây.

Bài tập 1:
Cho những khí: H, N, SO. Hãy cho biết:
a.Trong những khí trên, khí nào nhẹ hơn O và khí nào nặng hơn O. Tính cụ thể khí đó nhẹ hơn hay nặng hơn bao nhiêu lần?
b. Trong những khí trên, khí nào nhẹ hơn và khí nào nặng hơn không khí. Tính cụ thể khí đó nhẹ hơn hay nặng hơn bao nhiêu lần?
Lời giải:
a. Có khối lượng Mol của O là M = 32 g/mol
Do đó:
d = M/ M = 2/32 = 1/16 = 0.0625 => Khí H nhẹ hơn O và bằng 0.0625 lần O
d = M/ M = 14 / 32 = 0.4375 => Khí N nhẹ hơn O và bằng 0.4375 lần O
d = M/ M = 64 / 32 = 2 => Khí SO nặng hơn O 2 lần
b. Có khối lượng Mol của không khí là: M = 29
Do đó:
d = M / M = 2 / 29 ≈ 0.069 => Khí H nhẹ hơn không khí và bằng 0.069 lần không khí
d = M / M = 14 / 29 ≈ 0.483 => khí N nhẹ hơn không khí và bằng 0.483 lần không khí
d = M / M = 64 / 29 ≈ 2.2 => khí SO nặng gấp 2.2 lần không khí.
Xem thêm: FeCl2 màu gì, là chất gì? Tính chất vật lý và hóa học của FeCl2
Bài tập 2
Tìm khối lượng mol của khí có tỉ khối với H là 35.5
Lời giải:
Gọi khối lượng mol của khí cần tìm là M
Khi đó ta có:
d= M / M = M / 2 = 35.5
=> M = 70
Vậy khí có tỉ khối với H 35.5 có khối lượng mol là 70g/mol.
Trên đây là tổng hợp những kiến thức về tỉ khối hơi, công thức tính tỉ khối hơi và các kiểu bài tập vận dụng hay gặp nhất. Hi vọng với những kiến thức này các bạn đã có thể áp dụng vào việc học tập và nghiên cứu của mình một cách hiệu quả nhất.



