Mẫu nguyên tử bo là một trong những dạng bài tập rất thường hay gặp phải trong quá trình học và ôn luyện. Bài giảng mẫu nguyên tử bo là gì sau đây sẽ giúp các em hệ thống lại kiến thức về mẫu nguyên tử bo, cấu tạo nguyên tử và phương pháp làm bài tập một cách dễ dàng nhất.
Lý thuyết mẫu nguyên tử bo
Mẫu nguyên tử bo là gì?
Mẫu nguyên tử bo chính là sự phối hợp giữa mẫu nguyên tử Rutherford với 2 tiên đề Bo về trạng thái dừng, sự hấp thụ, bức xạ năng lượng nguyên tử và các quỹ đạo dừng.

Mô hình hành tinh nguyên tử
Sau nhiều năm nghiên cứu thì vào năm 1911, Rutherford đã thực hiện đề xuất lên mẫu hành tinh nguyên tử. Theo Rutherford, nguyên tử được cấu tạo bởi hạt nhân mang điện tích (+) được nằm ở giữa, xung quanh bao gồm những electron mang điện tích (-) được chuyển động trên quỹ đạo tròn hoặc quỹ đạo elip giống hệ Mặt Trời, vì vậy mà ta gọi là mẫu hành tinh nguyên tử.
Tuy nhiên, khó khăn của mẫu hành tinh nguyên tử này là không giải thích được sự tạo thành quang phổ vạch của các nguyên tử, cùng tính bền vững của nguyên tử.
Năm 1913, Bo đã vận dụng được thuyết lượng tử ánh sáng vào hệ thống nguyên tử, đề ra mẫu nguyên tử mới được gọi là mẫu nguyên tử Bo. Cho đến nay mẫu nguyên tử Bo vẫn giữ được mô hình hành tinh nguyên tử cùng với 2 tiên đề.
Tiên đề Bo về cấu tạo của nguyên tử
Tiên đề về các trạng thái dừng
Trạng thái dừng là khi nguyên tử chỉ tồn tại ở trong 1 vài trạng thái với năng lượng xác định là En. Thực chất các nguyên tử sẽ không bức xạ nếu như chúng đang ở trạng thái dừng.
Nguyên tử khi ở trạng thái cơ bản (n = 1) là trạng thái có năng lượng thấp nhất. Khi được hấp thụ năng lượng, nguyên tử ở trạng thái dừng sẽ có năng lượng cao hơn được gọi là trạng thái kích thích thứ n (n > 1).
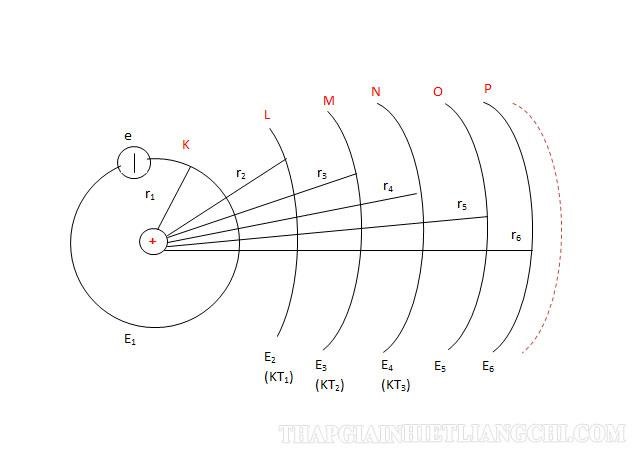
Ở trạng thái dừng của nguyên tử, các electron chuyển động quay quanh hạt nhân trên quỹ đạo có bán kính xác định hoàn toàn rn chính là quỹ đạo dừng.
- Tên của các quỹ đạo dừng
| Tên bán kính quỹ đạo | K | L | M | N | O | P |
| Số chỉ n | 1 | 2 | 3 | 4 | 5 | 6 |
| Bán kính | r0 | 4r0 | 9r0 | 16r0 | 25r0 | 36r0 |
| Mức năng lượng | E1 | E2 | E3 | E4 | E5 | E6 |
Bán kính bo rn = n2.r0 với r0 = 5,3.10-11, n là số nguyên tử, cũng bán kính quỹ đạo dừng của electron trong Hidro.
Xem thêm: Hạt nhân nguyên tử là gì? Kí hiệu, cấu tạo, điện tích hạt nhân nguyên tử
Tiền đề về bức xạ và hấp thụ năng lượng của nguyên tử
Nguyên tử khi chuyển sang trạng thái dừng năng lượng Em sang trạng thái dừng nhỏ hơn với năng lượng En sẽ làm phát ra phôtôn với mức năng lượng = hiệu của năng lượng Em – En.
Em – En = hfnm
Trường hợp nguyên tử ở trạng thái dừng có năng lượng En hấp thụ 1 phôtôn có năng lượng hf bằng hiệu của năng lượng Em – En thì sẽ chuyển năng lượng gọi là En là trạng thái dừng
Khi nguyên tử hấp thụ ánh sáng với bước sóng nào sẽ phát ra ánh sáng có cùng bước sóng đó.
Quang phổ phát xạ và sự hấp thụ của nguyên tử Hydro
Electron khi được chuyển từ mức năng lượng Ecao xuống mức năng lượng Ethấp sẽ làm phát ra 1 phôtôn với năng lượng xác định hoàn toàn: hf = Ecao – Ethấp.
Phôtôn tần số f ứng với sóng ánh sáng đơn sắc sẽ sở hữu bước sóng là λ = c/f, có nghĩa là ứng với vạch quang phổ có 1 màu nhất định.
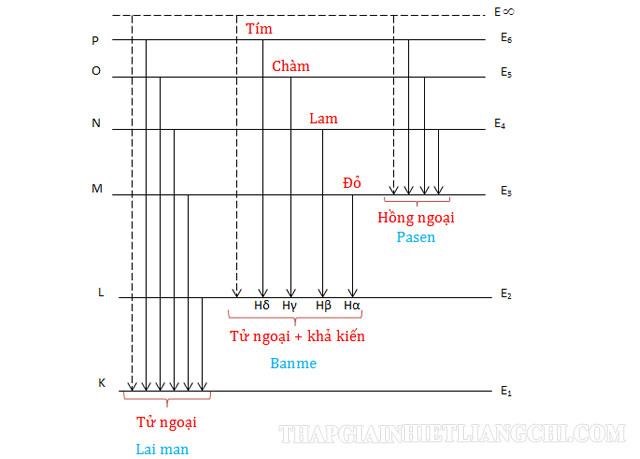
=> Quang phổ phát xạ chính là quang phổ của Hidro.
Giải thích cho sự tạo thành quang phổ vạch hấp thụ ta có:
Nếu như 1 nguyên tử hidro hiện đang ở mức năng lượng Ethấp mà vẫn nằm trong 1 chùm ánh sáng trắng, bao gồm tất cả các phôtôn với mức năng lượng từ nhỏ đến lớn khác nhau, thì nguyên tử đó sẽ hấp thụ 1 phôtôn với năng lượng phù hợp ε = Ecao – Ethấp ngay lập tức để nhằm chuyển thành mức năng lượng Ecao.
Một sóng ánh sáng đơn sắc bị hấp thụ sẽ khiến cho quang phổ liên tục bị xuất hiện vạch tối. Vì thế cho nên quang phổ hấp thụ nguyên tử hydro cũng chính là mẫu quang phổ vạch.
Một số bài tập về mẫu nguyên tử bo cơ bản
Bài 1: Hãy chỉ ra những điểm khác nhau cơ bản giữa mẫu nguyên tử Bo với mẫu nguyên tử Rutherford?
Hướng dẫn:
Các electron chuyển động quanh hạt nhân ở quỹ đạo có bán kính hoàn toàn xác định được gọi là quỹ đạo dừng. Đây là điểm khác nhau cơ bản giữa 2 mẫu nguyên tử trên.

Bài 2: Trạng thái dừng của nguyên tử dựa theo mẫu nguyên tử Bo là:
- Có thể là trạng thái kích thích hay cơ bản
- Chỉ ở trạng thái kích thích
- Trong nguyên tử thì các electron ngừng chuyển động
- Chỉ ở trạng thái cơ bản
Hướng dẫn:
Đáp án đúng là A.
Xem thêm: Phản ứng nhiệt hạch là gì? Ứng dụng, ví dụ phản ứng nhiệt hạch
Bài 3: Sự khác nhau cơ bản giữa mẫu nguyên tử Rutherford và Bohr là gì?
- Khác nhau về lực tương tác của hạt nhân nguyên tử với các electron
- Năng lượng được ổn định ở trạng thái dừng
- Là hình quỹ đạo của electron
- Mô hình nguyên tử có chứa các hạt nhân
Hướng dẫn:
Bohr giúp chỉ ra khái niệm trạng thái dừng là trạng thái có năng lượng ổn định. Còn Rutherford thì không
Vì thế đáp án đúng là B
Bài 4: Một nguyên tử H có bán kính quỹ đạo Bo thứ nhất là 0,53.10-10 m và bán kính quỹ đạo Bo thứ 5 bao nhiêu?
- 10,25.10-10 m
- 2,65.10-10 m
- 13,25.10-10 m
- 0,106.10-10 m
Hướng dẫn:
Bán kính quỹ đạo thứ là: r5 = 52 0,53.10-10 = 13,25.10-10 m
Vậy đáp án đúng là C
Bài 5: Trong nguyên tử Hidro có bán kính quỹ đạo dừng K là r0. Khi electron chuyển từ quỹ đạo dừng O xuống M bán kính sẽ bị giảm:
- 21r0
- 24r0
- 16r0
- 2r0
Hướng dẫn:
Quỹ đạo O có n = 5; M có n = 3
Suy ra rM = r09
rO = r025
Bán kính chuyển từ O về M, tương đương bán kính sẽ giảm đi 25 rO – 9rM = 16 r0
Đáp án đúng là C
Như vậy bài viết trên đây của chúng tôi đã giúp bạn đọc hiểu hơn về mẫu nguyên tử bo là gì, cũng như những điều cần biết về mẫu nguyên tử này. Đừng quên theo dõi chúng tôi để cập nhật thêm nhiều thông tin hữu ích nhé!



